- 藥監局通報藥品不合規 中國醫藥江蘇吳中旗下公司登榜
- 2020年07月24日來源:財經網
提要:國家藥品監督管理局網站公示的《國家藥監局關于25批次藥品不符合規定的通告》(2020年第50號)顯示,經河南省食品藥品檢驗所等9家藥品檢驗機構檢驗,有14家藥品生產企業生產的25批次藥品不符合規定。
昨日,國家藥品監督管理局網站公示的《國家藥監局關于25批次藥品不符合規定的通告》(2020年第50號)顯示,經河南省食品藥品檢驗所等9家藥品檢驗機構檢驗,有14家藥品生產企業生產的25批次藥品不符合規定。其中,江蘇吳中醫藥集團有限公司蘇州制藥廠、安徽國正藥業股份有限公司、湖南華納大藥廠股份有限公司、海南通用康力制藥有限公司、天津同仁堂集團股份有限公司生產的藥品均抽檢不合格;江蘇吳中醫藥集團有限公司系上市企業江蘇吳中實業股份有限公司全資子公司,海南通用康力制藥有限公司為上市企業中國醫藥健康產業股份有限公司旗下子公司,天津同仁堂集團股份有限公司為新三板掛牌企業。
上述抽查結果顯示,本次藥品檢驗經河南省食品藥品檢驗所、廣西壯族自治區食品藥品檢驗所、江蘇省食品藥品監督檢驗研究院、上海市食品藥品檢驗所、湖北省藥品監督檢驗研究院、中國食品藥品檢定研究院、四川省食品藥品檢驗檢測院、安徽省食品藥品檢驗研究院檢、大連市藥品檢驗檢測院9家藥品檢驗機構檢驗,共檢驗出14家藥品生產企業生產的25批次藥品不符合規定。
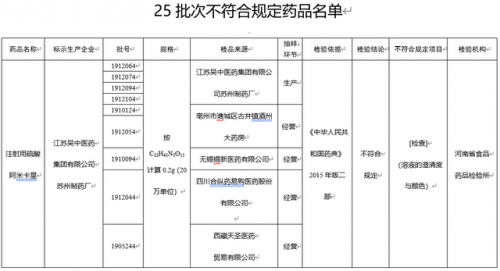
本次抽查發現,江蘇吳中醫藥集團有限公司蘇州制藥廠生產的9批次注射用硫酸阿米卡星經檢驗不合格。該藥品批號分別為1912064、1912074、1912094、1912104、1910124、1912054、1910094、1912044、1905244,規格為按C22H43N5O13計算0.2g(20萬單位),檢品來源及抽樣環節為江蘇吳中醫藥集團有限公司蘇州制藥廠生產、亳州市譙城區古井鎮酒州大藥房經營、無錫錫新醫藥有限公司經營、四川合縱藥易購醫藥股份有限公司經營、西藏天圣醫藥貿易有限公司經營,檢驗依據為《中華人民共和國藥典》2015年版二部,不符合規定項目為[檢查](溶液的澄清度與顏色),檢驗機構為河南省食品藥品檢驗所。
本次抽查發現,安徽國正藥業股份有限公司生產的復方愈創木酚磺酸鉀口服溶液經檢驗不合格。該藥品批號為19050801,規格為復方,檢品來源及抽樣環節為六安海王醫藥有限公司經營,檢驗依據為《國家藥品標準》化學藥品地方標準上升國家標準第十二冊及第十六冊,不符合規定項目為[檢查](裝量),檢驗機構為廣西壯族自治區食品藥品檢驗所。

本次抽查發現,湖南華納大藥廠股份有限公司生產的蘭索拉唑腸溶片經檢驗不合格。該藥品批號為190301,規格為15mg,檢品來源及抽樣環節為湖北森林藥業有限公司經營,檢驗依據為《中華人民共和國藥典》2015年版二部,不符合規定項目為[檢查](溶出度),檢驗機構為江蘇省食品藥品監督檢驗研究院。

本次抽查發現,海南通用康力制藥有限公司生產的4批次注射用奧扎格雷鈉經檢驗不合格。該藥品批號分別為21911021、21911022、21812032、21911012,規格為80mg(按奧扎格雷鈉計),檢品來源及抽樣環節為海南通用康力制藥有限公司生產,國藥控股溫州有限公司及合肥曼迪新藥業有限責任公司經營,檢驗依據為國家食品藥品監督管理局標準YBH14692005,不符合規定項目為[檢查](可見異物),檢驗機構為上海市食品藥品檢驗所。

本次抽查還發現,天津同仁堂集團股份有限公司生產的元胡止痛片經檢驗不合格。該藥品批號為JP24001,規格為片心重0.3克,檢品來源及抽樣環節為寧夏達美醫藥有限公司經營,檢驗依據為國家食品藥品監督管理總局藥品補充檢驗方法和檢驗項目批準件(批準件編號2014004),不符合規定項目為檢出金胺O,檢驗機構為四川省食品藥品檢驗檢測院。

溶液的澄清度是將藥品溶液與規定的濁度標準液相比較,用以檢查溶液的澄清程度;溶液的顏色是將藥物溶液的顏色與規定的標準比色液比較,或在規定的波長處測定其吸光度。溶液的澄清度與顏色可以在一定程度上反映藥物的純度,是一種能夠快速、簡便、準確進行藥品質量檢查的方法。
裝量系反映藥品重量或容量的指標,適用于固體、半固體、液體制劑,規定應按最低裝量檢查法進行檢查,不符合規定會導致臨床給藥劑量不足。溶出度系指活性藥物從制劑中溶出的速率和程度,不符合規定會影響藥物的吸收,降低生物利用度。
可見異物系指存在于注射劑、眼用液體制劑中,在規定的目視條件下能夠觀察到的不溶性物質,其粒徑或長度通常大于50微米。金胺O是一種色素或者染料,檢出該成分,提示有染色現象。
對不符合規定藥品,藥品監督管理部門已要求相關企業和單位采取暫停銷售使用、召回等風險控制措施,對不符合規定原因開展調查并切實進行整改。國家藥品監督管理局要求相關省級藥品監督管理部門依據《中華人民共和國藥品管理法》,組織對上述企業和單位生產銷售假劣藥品的違法行為立案調查,并按規定公開查處結果。
經中國經濟網記者查詢發現,江蘇吳中醫藥集團有限公司蘇州制藥廠成立于2006年2月14日,負責人為黃春榮。江蘇吳中醫藥集團有限公司為上市公司江蘇吳中實業股份有限公司控股的全資子公司、核心產業集團,是吳中醫藥產業基地骨干企業,蘇州市醫藥行業協會會長和江蘇省醫藥行業協會副會長單位。近三年(17-19年)集團銷售額平均約20億元,年均利稅超1億元。目前,吳中醫藥持有290余個藥品生產文號,20多項國家新藥證書,生產170個基因藥物、化學藥物和中藥品種。公司成立于2005年9月29日,注冊資本4億人民幣,姚建林為法定代表人、董事長。江蘇吳中實業股份有限公司成立于1994年6月28日,注冊資本7.12億元,于1999年4月1日在上交所掛牌,錢群英為法定代表人、總裁,錢群山為董事長,截至2020年3月31日,蘇州吳中投資控股有限公司為第一大股東,持股1.23億股,持股比例17.24%。蘇州吳中2019年年報顯示,報告期內,子公司吳中醫藥實現營收6.90億元,主營業務毛利4.89億元,總資產13.03億元,凈資產6.61億元,凈利潤5704.15萬元。
安徽國正藥業股份有限公司是于2003年12月通過重組方式設立的股份制企業,公司成立于1999年1月16日,注冊資本5350萬人民幣,朱立樹為法定代表人、實控人、總經理,萬毅為董事長,第一大股東為安徽泰元投資有限公司,持股比例84%,朱立樹為第三大股東,持股比例2%。朱立樹為安徽泰元投資有限公司法定代表人、實控人,與王冰共為第一大股東,持股25%比例股份。
湖南華納大藥廠股份有限公司是一家創新引領型藥品生產企業。公司自2001年創立以來,初步完成了從化學原料藥到化學藥物制劑、從藥材種植、植物提取分離到中藥制劑等化藥、中藥兩個產業鏈體系的配套規劃與建設,研發、生產、銷售在化藥、中藥等領域協調、有序發展。公司具體成立于2001年4月30日,注冊資本7030萬人民幣,黃本東為法定代表人、實控人、董事長兼總經理,湖南華納醫藥投資合伙企業(有限合伙)為第一大股東,持股比例53.08%。黃本東為湖南華納醫藥投資合伙企業(有限合伙)執行事務合伙人、大股東、實控人,持股比例64.67%。
海南通用康力制藥有限公司是中國通用技術(集團)控股有限責任公司旗下上市公司中國醫藥健康產業股份有限公司所屬的醫藥工業企業,是中國醫藥的一級利潤中心。2008年1月,中國通用技術集團通過吸收合并入主,兼并整合成立海南通用康力制藥有限公司,現有員工400余人,總占地面積80000多平方米。自創立以來,專注于高品質注射劑類(凍干粉針劑、無菌粉針劑、小容量水針劑)產品的研發、生產和銷售,現有文號111個,覆蓋10多個領域,產品聚焦心腦血管類、全身性抗感染類、能量合劑類,抗腫瘤類四大治療領域。公司成立于2000年5月16日,注冊資本5000萬人民幣,劉瑋為董事長、法定代表人,中國醫藥健康產業股份有限公司為大股東,持股比例54%。中國醫藥健康產業股份有限公司成立于1997年5月8日,注冊資本10.68億元,于1997年5月15日在上交所掛牌,高渝文為法定代表人、董事長,截至2020年3月31日,中國通用技術(集團)控股有限責任公司為第一大股東,持股4.41億股,持股比例41.27%。中國醫藥2019年年報顯示,海南通用康力制藥有限公司報告期內資產規模達到5.63億元,營業收入5.33億元,凈利潤4021.54萬元,經營活動現金流量8056.74萬元。
天津同仁堂集團旗下擁有“天津同仁堂”、“宏仁堂”兩個國家商務部首批認定的中華老字號品牌,“太陽”和“紅花”商標是國家工商總局認定的中國馳名商標,已發展成為集中成藥研發、生產和銷售為一體,以獨家藥品和原研藥品為特色的國家高新技術企業。公司成立于1981年10月8日,注冊資本1.10億人民幣,于2015年12月11日在新三板掛牌,主辦券商為長江證券股份有限公司。張彥森為法定代表人、董事長、實控人、大股東,持股比例41%。
版權及免責聲明:
1. 任何單位或個人認為南方企業新聞網的內容可能涉嫌侵犯其合法權益,應及時向南方企業新聞網書面反饋,并提供相關證明材料和理由,本網站在收到上述文件并審核后,會采取相應處理措施。
2. 南方企業新聞網對于任何包含、經由鏈接、下載或其它途徑所獲得的有關本網站的任何內容、信息或廣告,不聲明或保證其正確性或可靠性。用戶自行承擔使用本網站的風險。
3. 如因版權和其它問題需要同本網聯系的,請在文章刊發后30日內進行。聯系電話:01083834755 郵箱:news@senn.com.cn






