- 美泰彤:中國唯一一個擁有RA適應癥的甲氨蝶呤制劑
- 2024年08月07日來源:中國網
提要:近日,康哲藥業控股有限公司(下稱“康哲藥業”)甲氨蝶呤注射液(商品名:美泰彤®)增加適應癥的上市許可申請(NDA)獲得國家藥品監督管理局(NMPA)批準。甲氨蝶呤注射液獲批用于治療成人活動性類風濕關節炎(RA)。
近日,康哲藥業控股有限公司(下稱“康哲藥業”)甲氨蝶呤注射液(商品名:美泰彤?)增加適應癥的上市許可申請(NDA)獲得國家藥品監督管理局(NMPA)批準。甲氨蝶呤注射液獲批用于治療成人活動性類風濕關節炎(RA)。
康哲藥業于2024年8月5日獲得藥品注冊證書。作為中國首個以皮下給藥方式治療RA的預充式甲氨蝶呤注射液,本次獲批標志著甲氨蝶呤注射液在治療成人活動性類風濕關節炎(RA)領域取得重要進展,為患者帶來更安全、有效、便捷的治療選擇;同時,解決了中國RA患者MTX超適應癥用藥的問題,讓更多患者享受醫保報銷,增加藥物可及性。
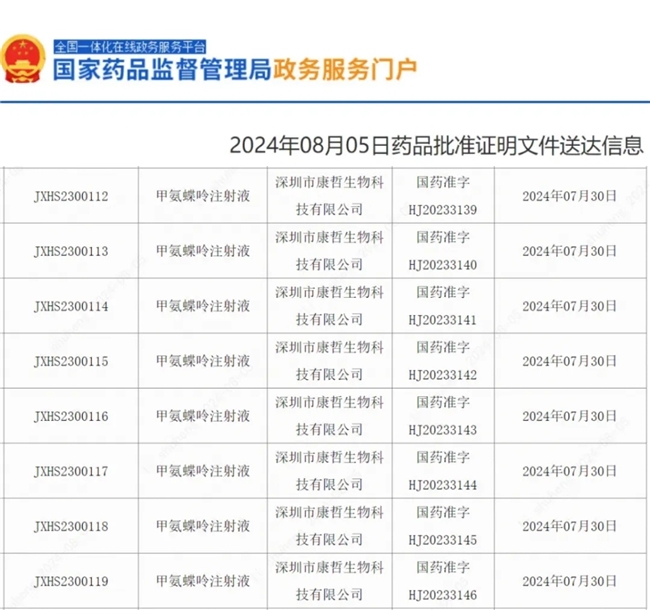
來源:國家藥品監督管理局官網
RA治療首選藥物
類風濕關節炎(Rheumatoid Arthritis, RA)作為慢性炎癥性自身免疫性疾病,主要影響關節,導致關節疼痛、腫脹、僵硬和功能喪失。據《類風濕關節炎診療規范》和《類風濕關節炎患者實踐指南》數據,中國類風濕關節炎患者約500萬人。
雖歷經更迭,甲氨蝶呤(MTX)依舊是RA治療錨定藥物。盡管其錨定地位曾面臨生物制劑挑戰,但2022版EULAR指南仍將MTX作為一線首選藥物,并繼續強調錨定地位。2024年4月20日發布的中國最新RA診療指南,同樣推薦MTX作為RA初始治療的首選藥物。
2021年美國風濕病學會針對類風濕關節炎治療的指南(下稱“指南”2021 American College of Rheumatology Guideline for the Treatment of Rheumatoid Arthritis),特別是關于疾病修飾性抗風濕藥物(DMARDs)的初始治療建議。它強調了甲氨蝶呤作為首選的單藥治療,并提供了在不同情況下的推薦方案。
指南明確指出,對于初治患者而言,強烈推薦MTX單藥治療,優于羥氯喹或柳氨磺吡啶,優于bDMARDs或tsDMARDs單藥治療,優于MTX 聯合一種非TNF-α類生物制劑或者tsDMARDs;有條件推薦甲氨蝶呤單藥治療,優于來氟米特,優于csDMARDs聯合治療,優于MTX聯合一種TNF-α類生物制劑。
作為有效的一線治療方案,MTX對于控制病情進展、改善患者生活質量具有重要意義。但長期以來,MTX在臨床上并未被充分利用。美國處方實踐調查分析顯示:劑量不足和用藥時間不足,影響了MTX在治療RA的作用。
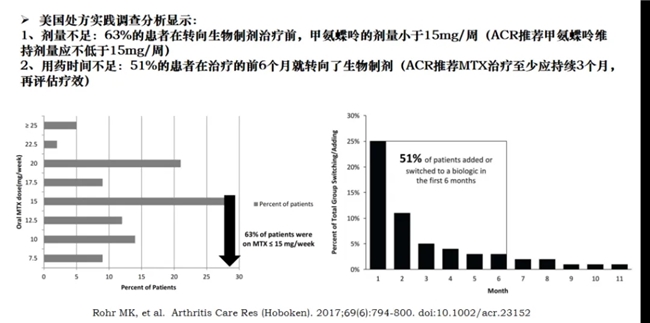
根據康哲藥業公開資料,甲氨蝶呤注射液(美泰彤?)是medac公司開發的多種規格的小容量甲氨蝶呤產品。
2020年9月,康哲藥業與medac公司簽訂許可協議,獲得了這款產品在中國大陸、香港地區、臺灣地區的開發和商業化獨家權益。2023年3月,該產品于中國獲批上市,用于治療成人嚴重、頑固、致殘性銀屑病。新增RA適應癥獲批后,可直接進入臨床應用,提高RA患者臨床治療生物利用度及便利性,減輕胃腸道副作用,同時降低患者治療負擔,滿足RA患者的基礎金標準用藥需求。
該產品已獲得瑞士、英國等21個歐洲國家主管部門批準,目前已在包括歐盟、澳大利亞和中國等在內的全球47個國家和地區上市。
臨床試驗成果顯著,療效與安全性兼備
甲氨蝶呤注射液產品采用皮下給藥,藥效更佳。如前述美國處方實踐調查分析顯示:劑量和用藥時間不足,影響MTX的作用。而口服轉皮下是提升用藥效果的重要方法。口服給藥的藥物暴露量在15mg/周達到平臺期,而皮下給藥的藥物暴露量呈線性增加,無藥物暴露限制。
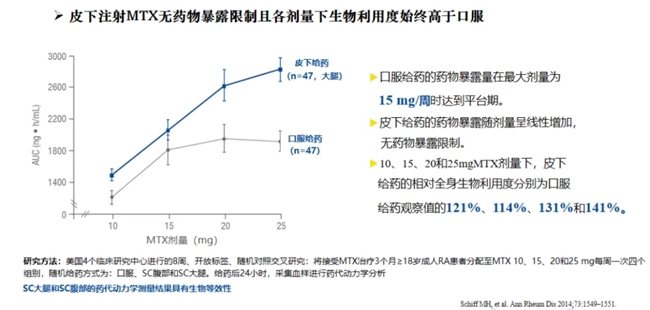
甲氨蝶呤注射液相較于口服MTX有更低的副作用,尤其胃腸道不良反應較少,在療效、良好的安全耐受性和依從性之間取得了更大的平衡。
該產品還易于使用,使患者可在家中自行給藥,賦予患者更多的控制權和獨立性,便于長期疾病管理。
在臨床研究中,甲氨蝶呤注射液的療效通過多個主要和次要終點進行了驗證。其中,主要終點是12周DAS28-ESR的變化量,結果顯示皮下注射方式相較于口服給藥具有顯著的優勢。此外,次要終點包括4、8、12周的DAS28-CRP變化值以及ACR20、ACR50、ACR70應答率,均表明了皮下注射方式的快速響應和療效。
根據中國III期臨床研究結果,甲氨蝶呤注射液在治療RA方面顯示出快速起效的特性,皮下注射更快,對于疾病活動度較高RA患者可以迅速控制病情。
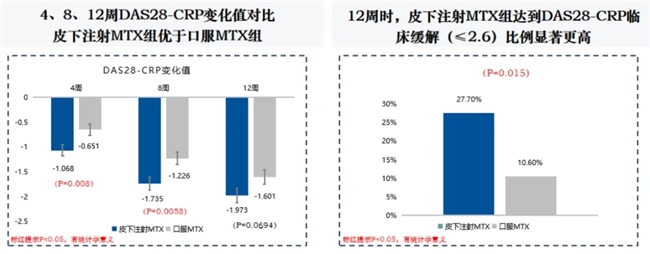
次要療效指標的結果顯示,產品與甲氨蝶呤片相比有療效更優的趨勢。研究結果還顯示,產品用藥早期即可觀察到的部分療效比甲氨蝶呤片更明顯,提示產品的療效出現時間更早。
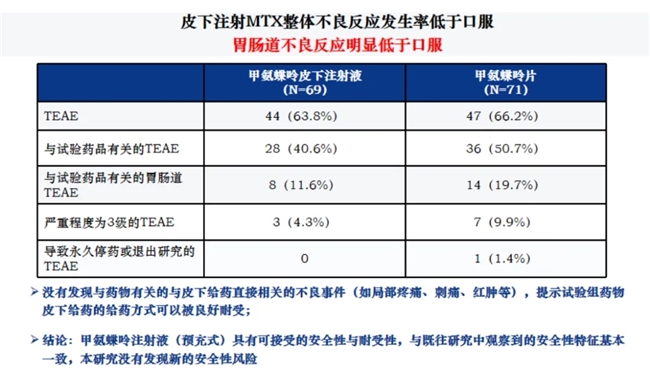
安全性方面,甲氨蝶呤注射液展現出了良好的耐受性和較低的不良反應發生率。特別是,它在胃腸道不良反應的發生率上明顯低于口服給藥,這為不能耐受口服治療的患者提供了另一種有效且安全的治療選擇。
除了臨床療效和安全性,甲氨蝶呤注射液的應用還可能對患者的日常生活質量產生積極影響。在臨床研究中觀察到,使用甲氨蝶呤注射液治療的患者在疼痛程度和健康評估問卷(HAQ-DI)評分上均有顯著改善。這意味著患者在日常生活中的疼痛得到緩解,功能受限減少,從而能夠更好地進行日常活動和工作。
甲氨蝶呤注射液作為中國首個以皮下給藥方式治療RA的預充式產品,不僅豐富了RA患者的治療選擇,更以其快速起效和高生物利用度,為成人活動性RA患者提供了有效的治療選項。
康哲藥業自1992年創立以來,始終堅持開放式商業化平臺和創新產品孵化平臺的雙輪驅動戰略,憑借敏銳的市場洞察力和強大的專家資源,不斷挖掘未滿足的臨床需求。目前,康哲藥業已布局30款創新產品,其中4款處于中國上市審評中。此次甲氨蝶呤注射液新增適應癥的獲批,是康哲藥業創新戰略的延續與深化,在創新發展道路上的又一里程碑。
結語
甲氨蝶呤注射液新適應癥的獲批,使RA的治療向更個性化、更精準邁進。其快速起效、高生物利用度以及較低的副作用,為RA患者提供了更為安全、有效且便捷的治療方案。同時,不再受超適應癥困擾,更多RA患者可以享受醫保報銷。
此外,甲氨蝶呤注射液的臨床研究結果令人鼓舞,不僅證實了其在療效上的顯著優勢,更在安全性和耐受性上展現了卓越的表現。為RA患者提供了更多選擇,同時也為醫生提供了更多的治療策略。
隨著這一適應癥的獲批,期待甲氨蝶呤注射液能夠迅速惠及更廣泛的RA患者群體,助其減輕病痛,改善生活質量,并最終實現更好的疾病控制。






